Découverte de ganglions axillaires métastatiques sans cancer primitif retrouvé (y compris après IRM mammaire)
– Effectuer un bilan d’extension complet et rechercher un primitif extra-mammaire (rôle fondamental de la TEP-TDM au 18FDG).
– Curage axillaire (avec recherche des récepteurs et de HER2 sur les ganglions)
– Traitement adjuvant classique
– Discuter la radiothérapie mammaire et ganglionnaire
-Si argument histologique pour une origine mammaire : radiothérapie sein, CMI, sus-claviculaire.
-Dans les autres cas : radiothérapie sus-claviculaire (et axillaire si adénecto- mie).
Cancer du sein bilatéral
Chacune des deux tumeurs est traitée comme un cancer unique en fonction de ses caractères anatomo-cliniques et évolutifs tant pour le traitement locorégional que pour le traitement adjuvant.
Cancer bifocal
Un cancer bifocal se définit par la présence de deux tumeurs séparées de plus de 2 cm.
• Traitement chirurgical
– Mastectomie totale avec preuve histologique sur les 2 lésions
– Option : un traitement conservateur peut-être proposé si l’exérèse des lésions est possible par une mastectomie partielle monobloc avec ou sans oncoplastie. Dans ce cas, une IRM préopératoire pour véri er l’absence d’autres lésions est à réaliser.
– L’évaluation ganglionnaire se fait par curage axillaire. En cas de bifocalité proche, un GS peut être proposé.
– Si la découverte de la bifocalité est histologique, il n’y a pas d’indication de curage de rattrapage.
• Traitements adjuvants
– Mêmes principes que pour les tumeurs unifocales
– La taille retenue est celle de la tumeur la plus volumineuse.
Cancer de la femme âgée
L’évaluation gériatrique est à discuter pour toute patiente de 70 ans et plus afin de repérer les critères de fragilité gériatrique: âge, perte d’appétit, perte de poids et/ou trouble de l’alimentation, indice de masse corporelle (IMC), perte d’autonomie physique (existence de dif culté(s) à̀ la marche), existence de troubles cognitifs connus ou d’une plainte cognitive ou de mémoire, (éléments dépressifs à l’interrogatoire), patiente polypathologique et/ou polymédication, etc.
La prise en charge se fait en association avec l’oncogériatre.
Il convient de proposer le traitement habituel, chaque fois que cela est possible.
Si cela n’est pas envisageable :
− tumeur RH+ : traitement anti-hormonal (TAM ou IA selon le ratio béné ce/ risque estimé)
− traitement local, radiothérapie classique ou hypofractionnée décidée au cas par cas.
Cancer du sein chez l’homme
Le cancer du sein chez l’homme est superposable à la prise en charge du cancer du sein chez la femme ménopausée à l’exception du traitement anti-hormonal.
Le bilan diagnostique est classique avec une mammographie, une échographie et dans certains cas une IRM. Il est nécessaire d’effectuer le même bilan d’extension avec écho abdominale, scintigraphie osseuse, TEP-TDM au 18F-FDG, marqueurs tumoraux avec les mêmes indications que chez les femmes atteintes de cancer du sein.
La mastectomie curage reste la stratégie thérapeutique de première intention mais il est possible pour une petite lésion de réaliser une tumorectomie ganglion sentinelle avec radiothérapie. La reconstruction mammaire est également possible.
La radiothérapie :
– Une radiothérapie pariétale est systématique dès que la tumeur est ≥ 1 cm et/ou pN+
– Elle est nécessaire en cas de traitement conservateur
– Le traitement local par radiothérapie exclusive est réservé aux formes les plus graves.
Les indications de la chimiothérapie sont les mêmes que chez la femme.
Le traitement anti-hormonal dans la plupart des cas est le tamoxifène pour une durée de 5 ans.
Un bilan oncogénétique (recherche de mutation de BRCA 1 et 2) ainsi qu’un bilan prostatique seront réalisés de manière systématique en raison de l’association fréquente entre la mutation BRCA2 et le cancer du sein .
Ecoulement mamelonnaire spontané unicanalaire (Voir: Ecoulements mamelonnaires)
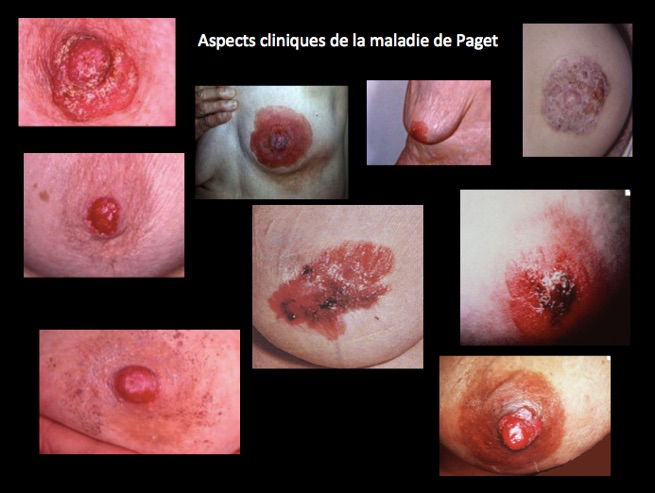
Maladie de Paget du mamelon
La maladie de Paget du mamelon est une pathologie rare, qui touche les femmes à partir de 40 ans. Elle représente 1 à 5% des cancers du sein. Il s’agit d’une forme particulière de cancer du sein qui se développe au niveau de la partie superficielle de la glande. Dans la plupart des cas, un cancer du sein sous-jacent est retrouvé mais il n’est palpable que dans 1/3 des cas. Ce dernier détermine le pronostic mais il n’y a jamais de connexion avec le mamelon.
Des cellules particulières épidermiques particulières ont été mises en évidence par Toker dans 10% des mamelons normaux. Ces cellules à cytoplasme abondant ont tendance à ébaucher des structures glandulaire et sont appelées cellules claires de Toker. Les rares cas on aucun carcinome sous jascent est retrouvé font supposer que la cellule de Paget pourrait provenir de l’hyperplasie des cellules de Toker. Les cellules normales de l’épiderme, claires, de grande taille , pourraient acquérie des signes de malignité histologique sous l’action d’un facteur carcinogène commun à celui du cancer mammaire soit sous l’influence de cytokines secrétées par le carcinome.
La maladie de Paget du mamelon se manifeste en général sur un seul mamelon comme suit : des rougeurs autour du mamelon, des démangeaisons, un mamelon épaissi et dur, des lésions pouvant faire initialement penser à un eczéma, un écoulement du mamelon, puis la formation de croûtes. L’évolution se fait en général de la partie centrale du mamelon vers la périphérie.
Le diagnostic nécessite une biopsie du mamelon. La recherche du cancer sous-jascent repose lr la mammographie, l’échographie et l’IRM si les autres examens sont négatifs. Si une lésion est retrouvée, elle sera bien sûr biopsiée.
1) En cas d’association à un adénocarcinome à distance de la plaque aréolo-mamelonnaire (PAM)
-Mastectomie totale d’emblée avec prélèvement ganglionnaire si invasif
— Traitement médical adjuvant et radiothérapie.
2) Sans anomalie clinique ou radiologique (IRM comprise) ou anomalie limitée à la région rétro-aréolaire
– Mastectomie centrale avec résection de la plaque aréolo-mamelonnaire (pamectomie) avec prélèvement ganglionnaire si lésion invasive
– Traitement médical adjuvant et radiothérapie.
Le cancer inflammatoire (T4d)
Le diagnostic est clinique et doit inclure les potentiels évolutifs.
• Définition du cancer inflammatoire
1. Il s’agit d’une définition clinique associée à une définition anatomopathologie
– la définition anatomopathologie sous-entend qu’il existe un diagnostic prouvé de cancer invasif du sein
– la définition clinique sous-entend qu’il existe des signes inflammatoires au niveau du sein (en partie ou en totalité) qui sont les signes de l’inflammation (érythème cutané, œdème, augmentation de la chaleur locale, douleur)
2. L’inflammation est généralement d’apparition et de progression rapide. Elle peut apparaître d’emblée ou sur une tumeur négligée témoignant d’une « poussée évolutive » (PEV). Cette notion de poussée évolutive (PEV) n’est toutefois pas reconnue par tous, et n’appartient pas à la classification TNM (qui ne définit que le T4d). On définit d’après la classification de l’Institut Gustave Roussy :
– la PEV 1 correspondant au doublement du volume tumoral en moins de 6 mois.
– la PEV 2 correspond à une inflammation d’une partie du sein.
– la PEV 3 correspond à une inflammation de tout le sein (mastite carcinomateuse).
• Chimiothérapie premières selon les protocoles classiques en fonction du type histologique de la tumeur. Le Trastuzumab est indiqué s en cas de HER2 positif.
• Traitement loco-régional: la mastectomie associée au curage axillaire reste nécessaire en cas de cancer inflammatoire suivie d’une irradiation loco-régionale.
Le cancer métastatique d’emblée
– Traitement médical premier à discuter en RCP et en fonction du statut HER2 et RH
– Traitement locorégional à discuter au cas par cas (mastectomie, traitement conservateur).
X-Antécédent de chirurgie esthétique du sein
En cas d’antécédent de chirurgie esthétique du sein (augmentation par prothèse par voie péri-aréolaire ou sous mammaire, réduction mammaire), il n’existe pas de contre-indication absolue au traitement conservateur voire à la technique du ganglion sentinelle.
Récidive
1- En cas de récidive invasive, il faut faire un bilan d’extension et la TEP-TDM au 18F-FDG est indiquée.
2-Récidive locorégionale isolée
Le traitement est à discuter en fonction de l’attitude thérapeutique initiale.
a) Récidive après traitement d’un carcinome canalaire in situ
-Si récidive après traitement conservateur: Mastectomie totale; le traitement conservateur est une option si récidive avec intervalle libre suffisant (> 5 ans), unique, < 2cm, +/- possibilités de radiothérapie complémentaire et selon âge versus espérance de vie.
-Si récidive après mastectomie totale
-Exérèse de la récidive + curage axillaire si récidive invasive
-En cas de récidive invasive, le traitement adjuvant (radiothérapie si non faite initialement, chimiothérapie, hormonothérapie, trastuzumab) se discute comme pour un cancer invasif d’emblée.
b)Récidive après traitement pour cancer invasif
-Le traitement locorégional :
-Si récidive locale intra-mammaire après mastectomie partielle:
– Mastectomie totale : discuter la possibilité d’une reconstruction mammaire immédiate.
– Si refus de la mastectomie par la patiente : chirurgie conservatrice si techniquement possible après IRM mammaire, essentiellement associée à une curiethérapie
– Radiothérapie en l’absence de radiothérapie antérieure.
– En cas d’impossibilité de traitement local : chimiothérapie et/ou traitement anti-hormonal.
-Si récidive de la région axillaire (ganglionnaire ou cutanée):
– Exérèse de la récidive avec exploration itérative du creux axillaire si possible
– Discuter la radiothérapie ganglionnaire si non faite antérieurement
-Si récidive de la paroi thoracique antérieure:
– Traitement local éventuel : chirurgie, radiothérapie ou chimiothérapie locale à discuter selon les cas
-Traitements complémentaires à discuter en fonction des facteurs pronostiques habituels, des thérapeutiques antérieures et de la durée d’intervalle libre.
3-Récidive locorégionale et/ou localisation secondaire à distance:
Le traitement est à discuter au cas par cas (voir traitement cas particuliers).
Cancer du sein et grossesse
L’association cancer du sein et grossesse est définie par la survenue d’un cancer pendant la grossesse et un an après l’accouchement.
Les cancers liés à une mutation délétère de BRCA1 ou de BRCA2 survenant à un âge plus précoce que les cancers sporadiques, certains de ces cancers peuvent logiquement être en rapport avec une telle mutation et un conseil génétique est à recommander à ces patientes.
A-Diagnostic
Le diagnostic clinique de cancer du sein est difficile lors de la grossesse ou lors de l’allaitement du fait modifications anatomiques du sein (augmentation de taille, hypervascularisation, engorgement) et aussi du fait que ni le praticien ni la patiente envisage volontiers le diagnostic. Une masse plus ou moins sensible, une atteinte cutanée, un écoulement a fortiori unique, canalaire et sanglant, doivent faire suspecter le diagnostic. Il s’agit le plus souvent d’une masse indolore mais les formes multifocale et bilatérales sont plus fréquentes. Les adénopathies axillaires, parfois prises pour des glandes mammaires accessoires, peuvent aussi être à l’origine du diagnostic. Il n’en reste pas moins vrai qu’il existe souvent un retard diagnostique ce qui fait que les formes avancées sont plus fréquentes qu’en dehors de la grossesse.
Le premier examen est l’échographie mammaire qui est sans danger. Si le diagnostic est positif, une mammographie bilatérale dans une seule incidence à la recherche de microcalcifications doit être proposée mais il faut savoir que la densité des glandes mammaires chez les femmes enceintes diminue la sensibilité de la mammographie. L’IRM peut être réalisée en cas de suspicion de multifocalité sur l’imagerie conventionnelle, avant de choisir entre une chimiothérapie néoadjuvante et une chirurgie. Elle n’est pas recommandée de façon systématique. L’IRM avec injection de gadolinium est parfaitement envisageable et ne comporte pas de risque particulier. Dans tous les cas le diagnostic doit être confirmé par biopsie (microbiopsie échoguidée le plus souvent). La majorité des cancers du sein associés à la grossesse sont des carcinomes canalaires infiltrants. La majorité de ces cancers sont de grade élevé et n’expriment pas les récepteurs hormonaux. L’amplification et/ou la surexpression forte de HER2 sont présentes dans près de 40 % des cas. Les cancers du sein associés à la grossesse sont donc des cancers généralement hautement proliférants. L’atteinte ganglionnaire est également plus fréquente et rend le pronostic plus mauvais que dans les cas hors grossesse.
B-Le bilan
Le bilan général comporte une radiographie pulmonaire (avec tablier de plomb), une échographie abdomino-pelvienne. Selon l’European Association of Nuclear Medicine, l’indication de la scintigraphie osseuse doit être pesée en fonction des bénéfices et des risques de cette procédure. Les doses reçues par un fœtus sont néanmoins très faibles (0,0063 mGy au niveau de l’utérus, 0,0046 mGy pour un fœtus de 8SA, 0,0026 pour un fœtus de 18SA) [http://www.eanm.org/scientific_info/guidelines)]. Elle peut être réalisée après l’accouchement et ne se justifie pendant la grossesse qu’en cas de suspicion de métastase osseuse modifiant la prise en charge thérapeutique.
C-Particularités thérapeutiques
1-La chirurgie
La grossesse a longtemps été considérée comme une contre-indication absolue à la conservation mammaire. Ceci n’est plus tout à fait le cas mais avec des réserves. Du fait du retard diagnostique, les femmes enceintes ont souvent un cancer du sein plus avancé que les patientes non enceintes, ce qui en fait plutôt des candidates à la mastectomie. Du fait de l’hypervascularisation du sein pendant la grossesse la chirurgie à tendance à être plus hémorragique rendant plus aléatoires les techniques de chirurgie oncoplastique. Par ailleurs, ces cancers survenant en moyenne à l’âge de 34 ans, il faut tenir compte avant toute décision de conservation, du risque élevé de rechute locale inhérent à cette tranche d’âge et du risque de multifocalité. Une imagerie exhaustive pré-opératoire bilatérale est indispensable (IRM). De même une reconstitution mammaire immédiate a peu de sens aussi du fait du volume mammaire controlatéral modifié par la grossesse.
La pratique du ganglion sentinelle est également contre-indiquée.
2-La radiothérapie
La radiothérapie est contre-indiquée pendant la grossesse mais elle peut être réalisée après l’accouchement.
3-Les traitements médicaux
La chimiothérapie est possible mais seulement après la fin du premier trimestre, soit dès 14 semaines. Un protocole à base d’anthracylines (jusqu’à 100 mg/m2 mais 50 mg/m2 dans la plupart des études) semble pouvoir être prescrit sans conséquences materno-fœtales majeures. Deux éléments doivent cependant être pris en compte :
-une dose de 50 mg/m2 d’anthracylines n’est pas optimale en particulier chez les patientes avec envahissement ganglionnaire ;
-L’ajout de taxanes améliore la survie mais en l’absence de données leur utilisation doit être évité en première intention.
Le Tamoxifène est tératogène et ne peut être donné qu’après l’accouchement. Les thérapeutiques ciblées comme le Trastuzumab sont également contre-indiquées. Il en est de même des biphosphonates.
Il n’existe pas de contre-indications aux antalgiques ou aux corticoïdes. Par contre, l’emploi des anti-inflammatoires non stéroïdiens est limité par les risques fœtaux.
D-L’interruption de grossesse
Elle se discute mais n’améliore pas le pronostic. Néanmoins, lorsque le diagnostic est posé avant 12 SA , la préservation de la grossesse entraîne un retard thérapeutique. Ce retard thérapeutique et ses conséquences doivent être clairement expliqués à la patiente.
E-L’accouchement
Si la grossesse est conservée, l’accouchement sera programmé. La date du déclenchement dépend de la date de découverte du cancer. Si le diagnostic est fait après 18 SA, l’accouchement se fera au-delà de 35 SA et si possible au-delà de 37 SA. Il est recommandé de ne pas réaliser de cure de chimiothérapie 2 à 3 semaines avant la date envisagée de l’accouchement pour minimiser le risque de neutropénie au moment de l’accouchement. Si le diagnostic est fait avant 18 semaines d’aménorrhée, l’accouchement doit être déclenché si possible à partir de 35 SA (parfois plus tôt si le diagnostic est fait tôt durant la grossesse) pour ne pas retarder les traitements complémentaires (taxanes, radiothérapie). La contraception à recommander est le stérilet au cuivre qu’on pourra poser environ 6 semaines après l’accouchement. Toutes les contraceptions hormonales sont contre-indiquées (même les stérilets à la progestérone). la contraception d’urgence est par contre possible.
En résumé, le traitement classique reste la mastectomie avec curage axillaire. Un traitement conservateur n’est envisageable que si la radiothérapie, qui sera faite après l’accouchement, n’est pas retardée.