
La toxoplasmose est une maladie parasitaire sans aucune gravité lorsqu’elle est contractée en dehors d’une grossesse.
Les symptômes en sont souvent tout à fait banals ou inapparents et c’est donc pendant la première consultation de la grossesse que l’on saura si vous êtes immunisée ou non.
Les statistiques indiquent que 60% à 80% des femmes sont immunisées avant leur première grossesse, n’impliquant alors aucun risque, puisque déjà immunisées.
Pour les 20 à 40% de femmes restant, le parcours de dépistage systématique et mensuel commence. L’incidence de la séroconversion pendant la grossesse est de 1,5%.
Le parasite, Toxoplasma Gondii, existe sous trois formes:
-Les trophozoïtes
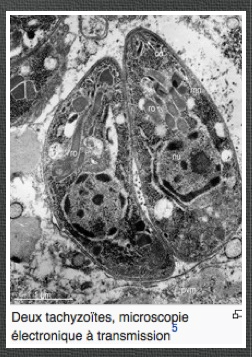
À multiplication rapide, détruisant la cellule hôte, c’est la forme observée à la phase initiale de l’affection. Ils sont rapidement détruits dès que les anticorps circulants apparaissent.
-Les kystes
Formes de résistance dans l’organisme infecté, les kystes se retrouvent dans des viandes de consommation et peuvent ainsi contaminer l’homme. Ils ne sont détruits que par des températures supérieures à 45 ° (forte cuisson) ou par une congélation prolongée. Ils résistent à la digestion peptique.
-Les oocystes :
C’est une forme de résistance qui est présente chez le chat qui n’a habituellement aucun symptôme et les rejette dans ses fèces. Ils deviennent infestant au bout de 2 à 3 jours et peuvent rester vivants plus d’un an dans le sol, représentant un autre mode de contamination humaine.
Le réservoir de parasites est donc tellurique et animal :
— oocystes pour le réservoir tellurique ;
— kystes pour le réservoir animal.

Le réservoir animal est représenté par toutes les espèces homéothermes herbivores, et surtout le mouton qui est particulièrement souvent infesté. Le chat se contamine surtout en chassant des oiseaux ou des souris, ou s’il mange de la viande saignante.
L’espèce humaine peu se contaminer de deux manières :
-par voie digestive et elle résulte de l’ingestion de viande parasitée consommée crue ou saignante, notamment le bœuf, le porc et le mouton, ou d’aliments ou de boissons souillés par les oocystes provenant des déjections de chats parasités. Le parasite ayant une durée de vie à l’extérieur d’un organisme assez impressionnant (1an dans la terre!), il peut également se trouver dans les légumes et dans les fruits frais.
-par voie hématogène :
-soit par injection (contamination accidentelle en laboratoire) ;
-soit par passage transplacentaire si la mère est infestée, risquant ainsi de contaminer le fœtus.
La maladie laisse persister une immunité durable, éliminant définitivement le risque d’une nouvelle contamination. Le taux de femmes immunisées contre la toxoplasmose est en France de l’ordre de 70 pour cent.
Il n’existe pas de vaccin qui protège contre la toxoplasmose, il faut l’avoir contracté pour être immunisée. Cependant, il existe des traitements qui permettent d’en atténuer les effets en cas de contamination en cour de grossesse.
Le danger de la toxoplasmose est surtout pour l’enfant, provoquant des lésions cérébrales et oculaires.
Cependant, si une grande vigilance s’impose, il ne faut pas céder à la panique. La contamination de la mère à l’enfant n’est pas systématique, et sa gravité diffère selon le stade de la grossesse. Pendant le premier trimestre, le risque de contamination est faible mais c’est dans cette période qu’elle est la plus dangereuse. Ensuite, les risques de contamination sont plus élevés, mais les séquelles seront moins sévères.
En pratique, si vous n’êtes pas immunisée, vous devrez faire, chaque mois, un examen sérologique afin de dépister au plus vite une éventuelle contamination. De plus il vous sera conseillé de prendre les mesures préventives suivantes :
1-Attention aux chats. Si vous avez un chat à la maison, ne changez pas sa litière vous-même, ou avec des gants, et ne le nourrissez pas avec de la viande crue. Ne vous faites pas griffer. Mais ne vous débarassez pas du chat!
2. Lavez vous les mains à chaque contact avec de la viande crue, de la terre ou des légumes et fruits qui viennent d’être cueillis.
3. Manger la viande bien cuite.
4. Lavez les légumes, les fruits, les salades et les plantes aromatiques avec encore plus de soins que d’habitude.
Interprétation de la sérologie toxoplasmique
L’interprétation de cette sérologie repose sur la comparaison des deux types d’anticorps dont il faut connaitre l’évolution en cas d’infection maternelle.
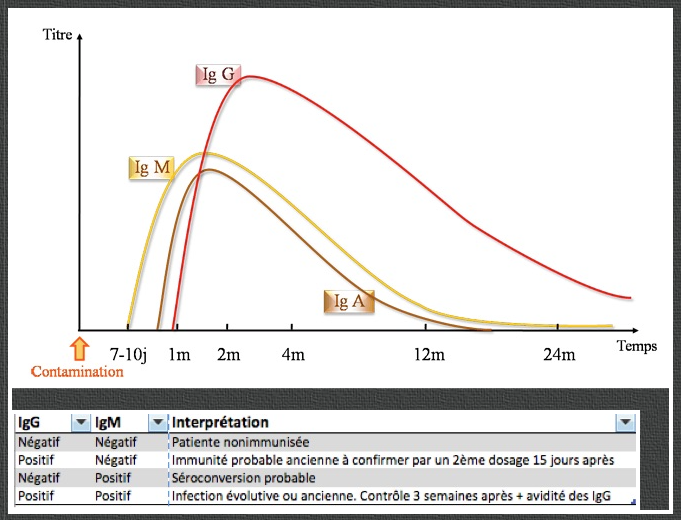
Lors d’une primo-infection:
Après une incubation moyenne de 16 jours, les anticorps apparaissent. Ils sont de deux types : IgG et IgM et leur évolution est différente.
–Les IgG atteignent leur taux maximum, en un temps qui peut aller de 2 jours à 3 semaines, mais le plus souvent en 8 jours. Le titre maximal est variable selon les sujets et selon les laboratoires et peut aller de 80 à plus de 1280. Ce n’est donc pas la valeur du titre qui a un intérêt mais son évolution.Ce titre reste ensuite stable très longtemps, pendant plusieurs mois ou plusieurs années et amorce ensuite une diminution lente. Il en résulte que si l’on peut saisir l’ascension des IgG, on ne peut saisir leur descente. Longtemps après, il persiste un taux résiduel de niveau très variable, pouvant être très bas, inférieur à 10, ou très élevé. Un taux d’IgG élevé n’est donc pas synonyme de Toxoplasmose récente.
-Les IgM : ils apparaissent en même temps que les IgG et ne persistent que 3 à 7 semaines.
-Des IgA apparaissent avant les IgG et se négativent assez vite.
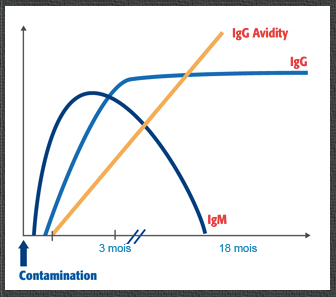
Lors d’une réinfection,
la réinfection ne survient que chez les sujets ayant un taux d’anticorps résiduels très bas. Les seuls signes sont sérologiques, marqués par une réascension du titre des anticorps (IgG). Cette réascension est plus rapide que lors de la primo-infection et elle ne concerne que les IgG. La contagiosité est possible mais de courte durée, correspondant au début de la remontée des anticorps.
Lorsque les IgG et les IgM sont positifs, il est important de savoir si l’infection date d’avant ou d’après la conception, soit en pratique de plus ou moins de 3 mois. On se sert pour cela d’un nouveau dosage 3 semaines après et de la mesure de l’avidité des igG. Si cette dernière est élevée cela correspond à une infection de plus de trois mois; l’avidité augmentant avec le temps. Les méthodes actuelles étant de plus en plus sensibles, il est possible de détecter de faibles taux résiduels d’une infection ancienne.
Les risques foetaux
L’atteinte fœtale est la conséquence non obligatoire de l’infection maternelle. Globalement, 70 % des enfants échappent à l’infection.
La fréquence et la gravité de l’atteinte fœtale dépendent de :
— la virulence de la souche du toxoplasme ;
— l’importance de la parasitémie maternelle qui est d’autant plus courte que son immunité humorale et cellulaire est efficace ;
— l’efficacité de la barrière placentaire ; elle est d’autant plus perméable que l’âge de la grossesse est avancé. Elle est excellente en début de grossesse. Ainsi le risque de contamination fœtale est de :
-1 % en période périconceptionnelle ;
-4 % de 6 à 17 semaines ;
-20 % de 17 à 28 semaines ;
-20 à 80 % de 28 semaines à terme ;
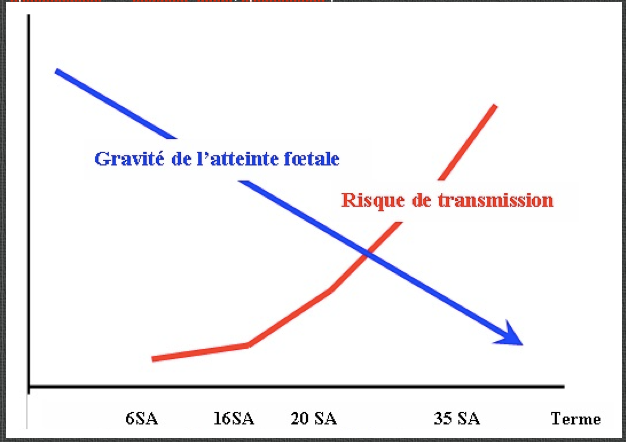
— la résistance du fœtus à l’infection et son aptitude à élaborer des anticorps dès le 2e trimestre. Cette notion va à l’encontre de la précédente. Cela veut dire qu’en début de grossesse il est très peu probable que le parasite passe du placenta au fœtus, mais s’il passe, l’atteinte sera très sévère en raison de l’immaturité immunologique de l’embryon ;
Le risque de transmission du parasite augmente avec le terme de la grossesse, à l’inverse de la gravité de l’atteinte fœtale qui diminue. La période la plus dangereuse pour le foetus se situe donc entre 10 et 24 semaines:
Les risques foetaux sont:
-avortement spontané;
-mort foetale in utéro;
-atteinte cérébrale: microcalcifications cérébrales, hydrocéphalie, microcéphalie;
-atteinte ophtalmique: surtout choriorétinite, mais aussi cataracte congénitale, microphtalmie;
-épanchements des séreuses: ascite, épanchement pleural.
Le diagnostic
Il repose sur le prélèvement de liquide amniotique: amniocentèse dès 18 semaines ou au moins 4 semaines après la contamination maternelle. Elle permet:
-la recherche par PCR de Toxoplasma Gondii;
-un test d’inoculation à la souris à la recherche d’une séroconversion 4 à 6 semaines après et de kystes toxoplasmiques à la dissection cérébrale. ce test est plus sensible que la PCR et peut rattraper quelques faux négatifs.
Prise en charge
1-Dès la séroconversion maternelle connue, on met en route un traitement maternel par la Spiramycine (Rovamycine® 3 millions d’unités 3 fois par jour, jusqu’à la fin de la grossesse quels que soient les autres résultats. Ce traitement vise à diminuer le pasage transplacentaire du parasite.
2-Puis, en fonction des résultats de l’amniocentèse:
a-si PCR négative et test d’inoculation à la souris négatif: on continue la Rovamycine et une surveillance échographique mensuelle à la recherche de signes de foetopathie. Une IRM céréblale anténatale peut être indiquée;
b-si la CR et la souris sont positif, il y a surement toxoplasmose congénitale on fait une échographie mensuelle + IRM foetale. S’il n’y a pas de signe de foetopathie, la grossesse est poursuivie et un traitement qui se veut curatif est mis en route jusqu’à l’accouchement:
-Pyriméthamine (Malocide ®) 50mg/j;
-Sulfadiazine (Adiazine®) 3g/j;
-Acide folique
-associés à la poursuite de la Rovamycine.
Si des signes échographiques de foetopathie apparaissent, un interruption médicale de grossesse peut être discutée.
Pour l’enfant
A la naissance, Il faut :
-analyser le placenta :
— pour examen anatomo-pathologique ;
— et bactériologique (inoculation à la souris) ;
-comparer la sérologie de l’enafant et de la mère :
— prélèvement au cordon pour recherche des IgM spécifiques ;
— prélèvement du sang maternel ;
— éventuellement par la suite, prélèvements du sang du nouveau-né ;
-examiner l’enfant :
— examen clinique général recherchant : ictère, hépatosplénomégalie, purpura ;
— demander une numération-formule sanguine ;
— rechercher des signes d’une encéphalite toxoplasmique congénitale : fond d’œil, radiographie du crâne, échographie transfontanellaire, scanner cérébral, ponction lombaire (augmentation de la protéinorachie).
-traiter l’enfant :
— s’il est normal et si l’infection est incertaine, au moins jusqu’aux résultats bactériologiques du placenta (3 à 6 semaines), par la spiramycine à la dose de 100 mg/kg/jour ;
— si l’atteinte fœtale a été confirmée, même si l’enfant est normal, pendant un an, en associant spiramycine, pyriméthamine (avec acide folinique) et sulfadiazine.
Une surveillance pédiatrique doit dans tous les cas être prévue jusqu’à l’âge de 10 ans car, même en cas de négativité de tous les examens, il n’est pas impossible de voir apparaître des lésions oculaires chez l’enfant quelques années plus tard.