La congélation du sperme humain a connu ses premiers succès dès les années 1950. Suivant les travaux chez l’animal menés dans les années 1970, c’est peu après l’avènement de la FIV que la cryoconservation des embryons humains a été développée, pour pallier le problème des embryons surnuméraires non transférés in utero. La possibilité de congeler les embryons a été proposée dès 1983. Il a été démontré que les embryons stockés dans l’azote liquide (-196°C) conservaient un potentiel évolutif.
Dans l’espèce humaine, les premières grossesses et naissances obtenues à partir d’ovocytes matures préalablement congelés, par une technique utilisant du DMSO comme cryoprotecteur, ont été rapportées à la fin des années 1980.
Intérêt de la congélation embryonnaire
Si le nombre d’embryons obtenu est supérieur au nombre d’embryons que l’on souhaite transférer, et il s’agit d’un maximum de deux en général, les autres embryons, appelés embryons surnuméraires, sont voués à la destruction. La congélation permet d’éviter ces pertes et de conserver des embryons, soit en vue d’une nouvelle grossesse après l’accouchement, soit en vue de nouveaux transferts s’il n’y a pas eu de grossesse. De plus ces transferts d’embryons congelés puis décongelés peuvent se faire sans nécessiter la lourde stimulation qui précède les ponctions pour fécondation in vitro.
La congélation trouve également un grand intérêt dans les situations suivantes :
– Utérus hypoplasiques ou mal formés impliquant le transfert d’un seul embryon à -chaque fois.
-Les hyperstimulations ovariennes sans projet de transfert d’embryon frais. En effet en cas s’hyperstimulation, la survenue d’une grossesse risque d’aggraver la situation, et il est préférable de repousser le transfert à un autre cycle et de congeler les embryons.
-Les endomètres inadéquats en cours de stimulation.
-les dons d’embryons (accueil d’embryons)
-La préservation du capital ovocytaire avant une chimiothérapie ou une radiothérapie.
Principes de la congélation
Les embryons surnuméraires peuvent être congelés à condition qu’ils soient de très bonne qualité . La congélation s’effectue classiquement au stade 4 cellules dans de l’azote liquide à -196° C.
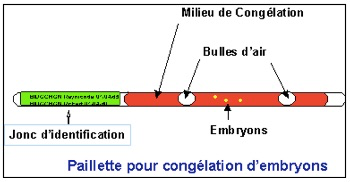
L’embryon, à ce stade, est constitué de plus de 90% d’eau. Il est donc nécessaire d’éviter la formation de cristaux de glace qui par augmentation de volume déchireraient les membranes cellulaires lors de la congélation. On élimine donc l’eau en la remplaçant par un cryoprotecteur, véritable « antigel » cellulaire. L’embryon est plongé dans des bains successifs contenant le cryoprotecteur et du sucrose à des concentrations différentes. Le sucrose rend le milieu hypertonique par rapport à l’embryon, ce qui entraîne la sortie de l’eau et la rentrée du cryoprotecteur. L’embryon est placé dans une paillette en plastique de 13 cm de longueur et de 2 mm de diamètre contenant un volume de 0,3 ml, une partie de la paillette contient toutes les indications nécessaires à une bonne identification.
La congélation s’effectue dans un appareil permettant une baisse de température progressive jusque vers -196°C.
La conservation des embryons se fait en azote liquide à -196°C et on a pu constater qu’après plusieurs années, les taux de survie après décongélation n’étaient pas modifiés.

Quels embryons congeler ?
D’un point de vue biologique, la congélation des embryons peut se faire à différents stades: lors des premières divisions cellulaires (2-4 blastomères) ou au stade du blastocyste. La congélation peut également se faire au stade du zygote, lorsque les 2 pronuclei sont présents (à ce stade, il ne s’agit pas encore d’un embryon).
Il faut tout de même savoir que tous les embryons surnuméraires ne sont pas congelables. On ne congèle en effet que ceux ayant une morphologie satisfaisante car les autres n’ont pratiquement aucune chance de supporter le cycle de congélation-décongélation. De plus, environ 10% des embryons congelés ne supportent pas la décongélation. En pratique, les 2/3 seulement des embryons congelés après 2 jours de culture retrouvent leur aspect morphologique initial et en outre leur taux de nidation est 3 fois plus faible que celui des embryons frais. Le taux de grossesses par transfert d’embryons congelés est donc d’environ 6 à 8 % si la congélation se fait à 2-3 jours de culture.
Par contre, les résultats sont toutefois bien meilleurs si l’on sélectionne les embryons à congeler par la culture prolongée, c’est-à-dire jusqu’au 5ème jour : ils sont plus souvent viables et la congélation-décongélation a moins d’effets néfastes à cause du nombre de leurs cellules. Cependant, la culture prolongée diminue le nombre d’embryons disponibles pour la congélation car un certain nombre d’entre eux, précisément ceux qui ne sont pas de qualité suffisante, ne vont pas atteindre le stade de morula ou de blastocyste. Le choix est donc, soit de congeler rapidement un plus grand nombre d’embryons sachant que certains ne supporteront pas la décongélation, soit prolonger la culture sachant qu’il y aura moins d’embryons mais de meilleure qualité et supportant bien la décongélation avec des taux de grossesse comparables à ceux obtenus par transfert d’embryons frais.
Si vous refusez la congélation, vous devez en aviser l’équipe médicale avant la tentative de FIV. Dans ce cas, il ne sera mis à féconder qu’un nombre limité d’ovocytes (correspondant au nombre maximal d’embryons transférés). Un accord écrit vous sera demandé (vous et votre conjoint si vous êtes mariés) pour la congélation et lors de chaque décongélation. Vous devrez renouveler votre accord tous les ans pour maintenir la congélation des embryons et cela pour une durée maximum de cinq ans.
La décongélation
La paillette contenant l’embryon est sortie de l’azote liquide. Dès lors il faut réhydrater l’embryon par des bains successifs contenant de moins en moins de cryoprotecteur et de plus en plus de milieu aqueux, à une température de +37°C.
Les embryons ayant survécu au procédé congélation – décongélation sont transférés le jour même de la décongélation.
Le transfert des embryons congelés
Un bilan préalable d’évaluation de l’endomètre est indiqué pour le succès de l’implantation. En fonction de ce bilan, le clinicien
pourra opter pour l’une des solutions suivantes :
Cycles spontanés : Si la patiente présente des cycles naturels de bonne qualité, il est possible, sans traitement particulier de suivre l’évolution du cycle afin de bien contrôler l’évolution et la qualité du follicule obtenu naturellement. Dans ce cas, le cycle de la patiente est surveillé par échographie et dosage d’œstradiol afin de repérer le jour de l’ovulation
Cycles Stimulés : Dans certaines conditions on pourra effectuer une légère stimulation ovarienne avec déclenchement programmée de l’ovulation et contrôle de l’aspect de l’utérus.
Cycles substitués (ou artificiels) : Dans Ce dernier cas de figure, en l’absence de cycle, on pourra créer un cycle artificiel en 2 temps, en utilisant l’œstradiol et la progestérone associés souvent à des traitements de complémentation (agoniste, HCG).
Le choix entre les techniques se fait essentiellement en fonction de la qualité de l’ovulation de la patiente.
Le transfert s’effectuera généralement en fonction de l’âge des embryons de J3 à J5 après le déclenchement de l’ovulation.
Le transfert de blastocyste se fera dans des conditions similaires.
Le transfert lui-même se fait dans les mêmes conditions que pour les embryons non congelés.
Le concept de fenêtre d’implantation est très important pour développer des protocoles de TEC/DO efficaces. La réceptivité utérine est classiquement considérée maximale à j17-19 du cycle naturel, et sa durée est limitée à 48 heures. Il semble que la réceptivité endométriale est acquise après 2 jours de substitution pour être ensuite maintenue pendant 4 jours. Il a été aussi suggéré que dans les cycles stimulés ou préparés artificiellement, une avance ou un retard de la fenêtre d’implantation est possible par rapport au cycle naturel.
Les protocoles de TEC peuvent être effectués en cycle naturel, en cycle stimulé ou avec l’aide d’un cycle complètement artificiel. L’avantage évident du cycle naturel est que la préparation ne nécessite pas de médication particulière, ce qui réduit le coût. En revanche, il n’est indiqué que pour les femmes ayant des cycles réguliers avec ovulation prouvée. Le « timing » peut s’avérer difficile, et un monitorage échographique strict ainsi que la détection exacte du pic de LH par prélèvements sanguins ou test urinaire deviennent aussi nécessaires. Pour circonvenir ces problèmes, une alternative est le cycle stimulé par citrate de clomifène et/ou gonadotrophines. Néanmoins même avec cette méthode, le taux d’annulation peut être considérable, et le citrate de clomifène pourrait avoir des effets indésirables sur l’endomètre.
En revanche, l’utilisation d’un cycle artificiel avec administration d’estrogènes et de progestérone exogènes (avec ou sans agoniste de GnRH) donne un contrôle parfait sans nécessité de monitorage exhaustif. L’administration préalable d’agoniste de GnRH permet encore davantage de flexibilité, car il permet d’allonger la phase folliculaire de la préparation selon les besoins individuels de la patiente et/ou de l’équipe. Par ailleurs, la préparation hormonale est plus chère par rapport aux autres alternatives (surtout en cas de l’addition de l’agoniste).
Les comparaisons entre les différents régimes de TEC sont difficiles du fait qu’actuellement il y a encore peu d’études randomisées disponibles et on considère actuellement qu’aucun régime n’a démontré sa supériorité. Par conséquent, pour les femmes avec des cycles ovulatoires, les régimes naturels comme artificiels peuvent être également proposés. Lorsqu’un régime artificiel est choisi, l’administration de l’agoniste du GnRH semble apporter un bénéfice
Dans tous les cas la progestérone naturelle est utilisée comme support de la phase lutéale dans les cycles de FIV ainsi que pour obtenir la transformation sécrétoire de l’endomètre dans les cycles de transfert d’embryons congelés.
«Les embryons orphelins »
Les embryons congelés peuvent devenir abandonnés ou orphelins:
-si vous décidez de ne pas envisager d’autre grossesse durant les cinq ans de conservation ;
-si vous ne renouvelez pas l’autorisation annuelle de prolongation de la congélation ;
-ou au bout de cinq ans de conservation.
Dans tous ces cas, il est prévu qu’ils puissent être détruits ou encore donnés à un autre couple, toujours avec l’accord des géniteurs. D’autres peuvent être « orphelins » par suite du décès de la conjointe ou des deux membres du couple. Au total, ces embryons non réclamés sont peu nombreux, 1 à 5 % des embryons congelés. Mais sans la congélation, il y aurait encore plus d’embryons abandonnés : tous les embryons surnuméraires.
Attention : un couple dont des embryons ont été conservés ne peut bénéficier d’une nouvelle tentative de fécondation in vitro avant le transfert de ceux-ci sauf si un problème de qualité affecte ces embryons.