Qu’est-ce que l’endométriose?
L’endométriose est une maladie gynécologique fréquente puisqu’elle concerne 15% des femmes en âge de procréer et qu’on la retrouve sur près de 40% des pièces opératoires d’hystérectomies. Elle se caractérise par le développement, hors de la cavité utérine, de fragments de muqueuse utérine donc d’endomètre. Ces lésions endométriales présentent les mêmes caraactéristiques que la muqueuse utérine et, comme elle, sont sensibles à l’action des œstrogènaes. L’endométriose est donc une maladie œstrogéno-dépendante. C’est pourquoi elle se manifeste chez les femmes en âge de procréer (c’est-à-dire en période d’activité génitale), parfois dès l’adolescence. Il s’agit en outre d’une maladie fortement adhésiogène provoquant des séquelles adhérencielles entres divers organes atteints.
Les localisations de l’endométriose
On distingue des localisations utéro-annexielles, des localisations dites superficielles et des localisations dites profondes.
A-L’endométriose utéro-annexielle concerne l’appareil génital:
-Sa présence au niveau de l’utérus s’appelle l’adénomyose. Elle est quasi constante dans tous les cas d’endométriose et se traduit par une dysménorrhée invalidante et ds métrorragies.
-L’atteinte ovarienne provoque des kystes endométriosiques appelés endométriomes qui sont généralement asymptomatiques sauf en cas d’hémorragie intrakystique ou de rupture. Ils provoquent une baisse de la réserve ovarienne lorsqu’ils dépassent une taille de 6cm.
-Les trompes sont atteintes par des phénomènes adhérenciels source d’obturation tubaire, d’hydrosalpinx ou d’hématosalpinx.
B-L’endométriose dite superficielle
est l’atteinte -superficielle- du péritoine sous la forme de micro-implants millimétriques, possible partout mais avec une préférence pour le cul de sac de Douglas, les utéro-sacrés et les ligaments larges.
C-L’endométriose profonde
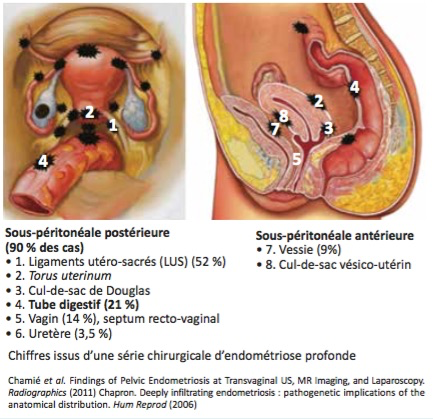
Elle se définie par l’infiltration en profondeur, sous le péritoine, au-delà de 5cm, ou par l’atteinte des structures musculaires lisses environnant l’utérus. Cela concerne deux territoires: l’espace sous-péritonéal postérieur et l’espace sous-péritonéal antérieur. ce type d’endométriose est le moins souvent diafnostiqué alors qu’il est responsable des symptômes les plus invalidants, souvent chroniques et à récrudescence cataméniale. Sont évocateurs: dyspareunie profonde, exonération douloureuse, dyschésie rectale, rectorragies, dysurie, hématurie, voire hydronéphrose par atteinte urétérale.
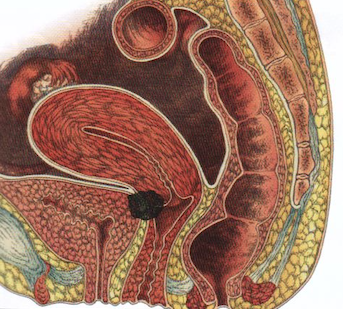
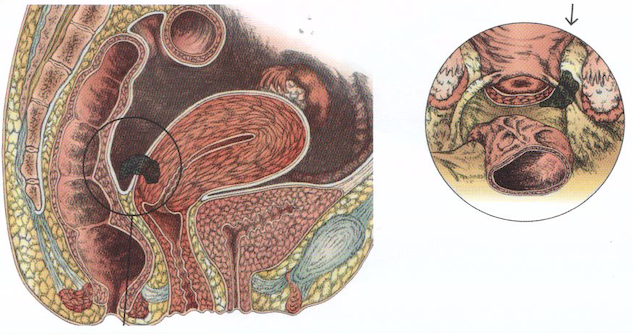
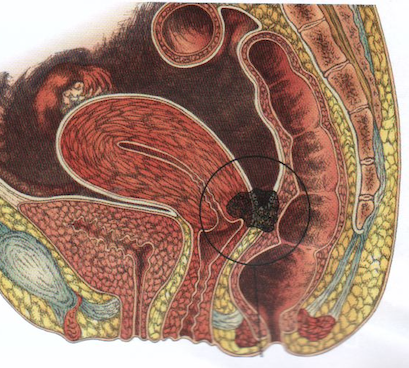
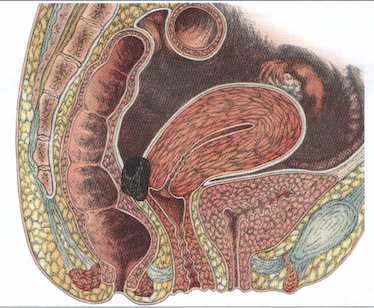
D-Localisations plus rares:
col de l’utérus, vagin, vulve, paroi abdominale (vers l’ombilic, le creux de l’aine ou dans une zone présentant des cicatrices), épiploon. Exceptionnellement, des lésions d’endométriose peuvent même apparaître sur des organes à distance de l’utérus comme la plèvre, les poumons).
Physiopathologie
La physiopathologie de l’endométriose est complexe, probablement multifactorielle et toujours l’objet de discussions. Diverses théories ont été ptoposées:
Théorie de la greffe péritonéale: reflux menstruel, métastases lymphatiques ou vasculaires
Théorie de la métaplasie à partir de cellules d’origine coelomique (totipotentes), sous l’effet de substances libérées par l’endomètre, des stimuli hormonaux ou infectieux
Théorie embryogénétique: à partir de restes embryonnaires ectopiques
Théorie du déficit immunitaire
Il semble de plus exister un «terrain» favorable à l’endométriose: Femmes perfectionnistes, fines, inteligentes; Caucasiennes et asiatiques; après des traumatismes affectifs; facteur familial…
Le diagnostic de l’endométriose
Elle concerne une femme sur 7, mais toutes n’en souffrent pas et beaucoup d’endométrioses n’entraînent aucun trouble. L’un des problèmes tient au fait qu’une endométriose peut se manifester par des symptômes très divers. Dans certains cas, ce sont les douleurs qui prédominent, dans d’autres cas la maladie provoque une infertilité, des perturbations d’autres organes (par exemple urinaires ou intestinales) ou bien elle engendre lentement et progressivement des lésions des organes internes, en restant totalement méconnue. La diversité des manifestations cliniques explique certainement le fait que l’endométriose n’est souvent découverte qu’au bout de plusieurs années, avec un retard en moyenne de 7 à 9 ans. A l’inverse, on voit souvent des diagnostics d’endométriose portés par excès uniquement sur de tels signes. En effet, combien de femmes n’ont jamais eu de douleurs au moment des règles, ou n’ont jamais de lourdeurs dans le bas ventre?
A-L’interrogatoire est toutefois une étape importante et on retiendra la règle des trois D:
-Dysménorrhée
-Dyspareunie
-Dyschésie rectale
-Dysurie douloureuse
-Douleurs pelviennes chroniques
-Dysfertilité
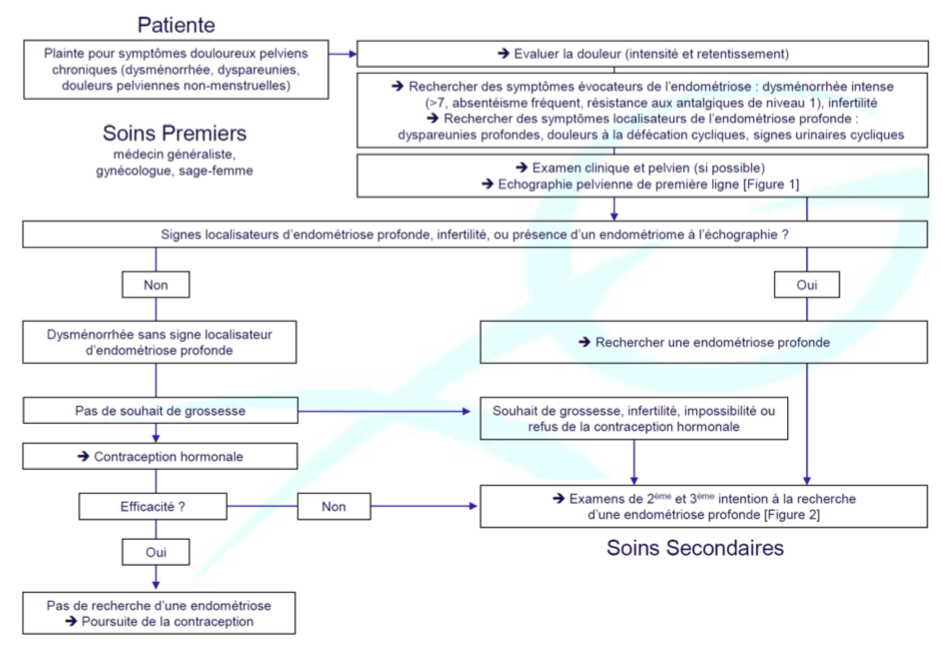
D-Le diagnostic de l’endométriose
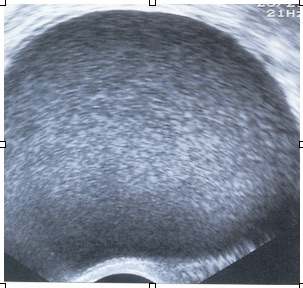
a-L’échographie pelvienne, par voie vaginale
L’échographie endovaginale est l’examen de 1re intention, bien qu’elle ne soit pas toujours suffisamment sensible, notamment pour les atteintes latéropelviennes. Elle doit surtout s’attacher à la recherche de l’endométriose profonde qui est potentiellement la plus grave et qui représente la partie immergée de l’iceberg. On recherche les images directes de foyers endométriosiques, en particulier au niveau des sites préférentiels de la maladie:
-L’espace sous-péritonéal postérieur est le plus souvent concerné. Sous et en arrière de l’utérus, ce sont: les ligaments utéro-sacrés (surtout le gauche), le rectum, le cul de sac vaginal postérieur, la jonction recto-sigmoïdienne (à hauteur du fond utérin) et le sigmoïde. seul le carrefour iléo-caeco-appendiculaire est plus difficile d’accès.
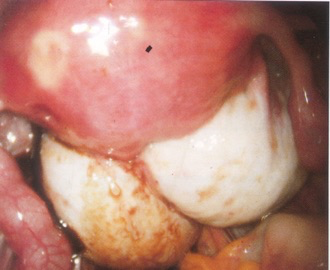
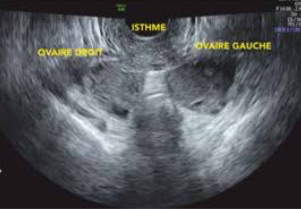
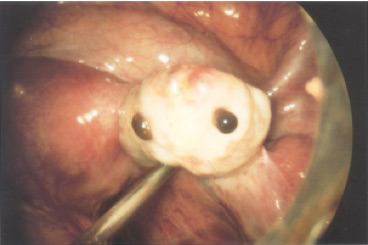
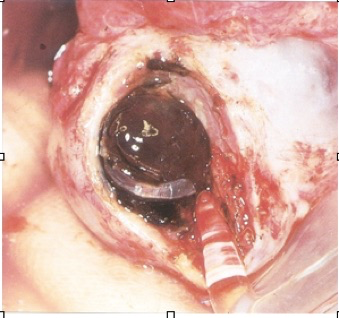
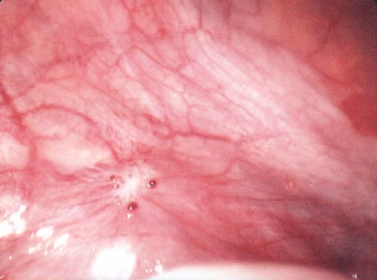
-l’espace sous-péritonéal antérieur, moins souvent concerné avec la cloison vésico-utérine (et envahissement possible de la paroi vésicale).
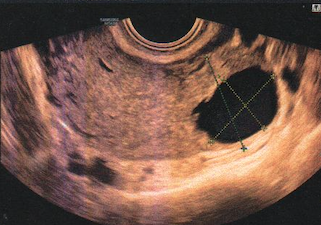
On recherche aussi l’absence de mobilité de l’utérus par rapport au rectum, au sigmoïde, aux ovaires et à la vessie du fait du caractère fortement adhésiogène de l’endométriose. A l’aide des mouvements de la main abdominale et de la sonde vaginale, on provoque «le signe du glissement» qui s’il est positif témoigne de la bonne mobilité de l’utérus par rapport aux structures digestives, donc de la non oblitération partielle ou complète du Douglas et donc de l’absence d’atteinte de l’espace péritonéal postérieur. D’autres conséquences du caractère adhésiogène est la possibilité d’observer un hydro ou un hématosalpinx, un pseudo-kyste péritonéal ou des ovaires accollés («Kissing ovaries»). Un endométriome sera facile à voir sous la forme d’un kyste, jamais parfaitement rond ,à contenu finement et régulièrement échogène, non vascularisé au Doppler et avec parfois des dépôts punctiformes, millimétiques, hyperéchogènes, surtout périphériques traduisant l’hémosidérine.
b-L’IRM
L’échographie pelvienne et l’IRM et ne permettent pas un diagnostic satisfaisant des lésions d’endométriose superficielle. La réalisation de ces examens n’est pas recommandée dans le but d’éliminer une forme superficielle ou débutante de la maladie.
b-L’iRM pelvienne
L’IRM pelvienne est l’examen de référence, avec une excellente sensibilité, mais un défaut relatif de spécificité, entre autres pour les ligaments utérosacrés. Cela signifie qu’il peut y avoir un certain nombre de faux positifs, variable là encore selon l’expertise des radiologues.
L’IRM est toutefois la technique de référence, permettant une cartographie exhaustive des lésions et une classification radiologique du degré d’extension avec un score prédictif de la complexité chirurgicale à envisager..
Devant une suspicion clinique d’atteinte extrapelvienne, une entéro-IRM peut être réalisée pour les atteintes iléocæcales, et une IRM diaphragmatique pour les atteintes de l’hypocondre droit.
Pour le diagnostic positif de l’endométriose profonde, une IRM pelvienne positive est moins performante que la chirurgie en raison du nombre de faux-positifs d’environ 23 %, si l’on tient compte de l’ensemble des aspects, en particulier l’épaississement isolé des ligaments utérosacrés. La présence de signaux caractéristiques en IRM (présence de spots en hyper signaux T1) permet, en revanche, une certitude diagnostique.
D-L’adénomyose
Définition
L’adénomyose (ou endométriose utérine) est une affection gynécologique caractérisée par la présence de glandes endométriales et de tissu de support (stroma cytogène) dans le myomètre (paroi musculaire de l’utérus). Ces implants endométriaux peuvent correspondre à des diverticules (sortes de petites poches reliées à la cavité utérine) ou à des îlots sans continuité avec la cavité utérine. Après que ce tissu de glandes ait subit la croissance pendant le cycle menstruel, lorsqu’il doit s’éliminer au cours des règles, le sang et les vieux tissus ont beaucoup de mal, voire ne peuvent pas sortir du muscle, ce qui provoque des douleurs utérines sous forme de crampes menstruelles.
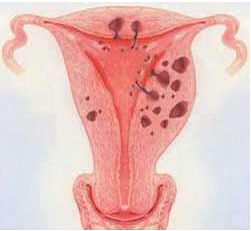
Signes de l’adénomyose
Dans environ 40% des cas d’adénomyose, les femmes ne présentent aucun symptôme, mais lorsqu’ils existent, ceux-ci sont semblables à l’endométriose. On retrouve ainsi par ordre de fréquence : des ménorragies (menstruations abondantes et prolongées), dysménorrhées (douleurs menstruelles), métrorragies (écoulements sanguins en dehors des règles), pesanteur pelvienne, dyspareunies profondes (douleurs pendant les rapports sexuels).
diagnostic de l’adénomyose
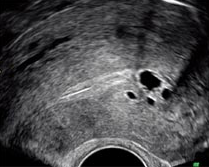
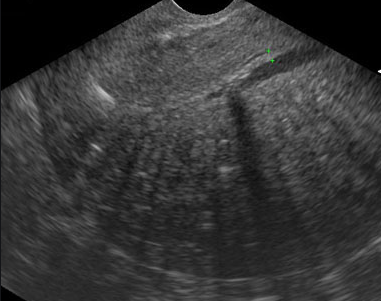
L’adénomyose dont on a dit qu’elle était quasi constante, se traduit sur une échographie endovaginale par un utérus globuleux, augmenté de volume avec un myométre épais et une asymétrie entre ses faces postérieure et antérieure (la face postérieure étant plus épaisse). Il y a de petites images cavitaires intra-myométriales, des images nodulaires intra-myométriales hyperéchogènes et un myomètre hétérogène. On peut parler d’adénomyome lorsque ces cavités sont volumineuses.
Traitement de l’adénomyose
L’adénomyose asymptomatique ne doit ni être traitée ni être surveillée. Divers traitements peuvent être essayés mais ne sont pas toujours efficaces à 100%. Les méthodes les plus effaces sont: une pilule estroprogestative prise en continu (donc sans règles) ou un traitement (macro)progestatif seul en continu (sans règles également), aussi un stérilet à la progestérone type Mirena®, voire les agonistes de la Gn-RH créant (provisoirement) une ménopause artificielle, éventuellement avec ad-back therapy. L’add-back therapy consiste à réintroduire un peu d’oestrogènes : suffisamment pour pallier les effets secondaires générés par l’analogue Gn-RH mais insuffisamment pour agir sur les cellules (hormono-dépendantes à l’œstrogène). L’add-back therapy améliore le confort pour ce type de traitement.
En cas d’échec et surtout si la femme ne souhaite plus de grossesse, le traitement radical est l’hystérectomie, au mieux réalisée par voie vaginale (possible en ambulatoire – voir le chapitre consacré à l’hystérectomie). cette opération règle la question de l’adénomyose mais ne traite pas les signes d’une endométriose pelvienne ou abdominale associée.
D-Autres examens
-Le coloscanner à l’eau est utile en pré-opératoire avant une chirurgie d’exérèse radicale pour une localisation recto-sigmoïdienne.
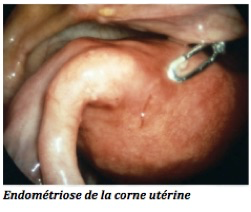
-La coelioscopie n’a plus d’intérêt, à titre diagnostique de la maladie, car elle ne montre au mieux que des nodules d’endométiose superficielle qui ne sont que la part émergée de l’iceberg. Elle reste utile en cas d’infertilité. En cas de coelioscopie, le compte rendu opératoire doit décrire la taille, l’aspect macroscopique, la localisation et l’infiltration en profondeur de toutes les lésions ainsi que les adhérences . Dans la prise en charge de l’infertilité, la référence aux classifications reconnues apparaît souhaitable . Il n’y a pas de données permettant d’affirmer la supériorité d’une des classifications. Il est souhaitable de réaliser dans le même temps opératoire la phase diagnostique et la phase thérapeutique de l’endométriose. Cependant, en cas de découverte au cours de la cœlioscopie d’une lésion dont le traitement présente des risques chirurgicaux, il peut être préférable de renoncer à son traitement afin de compléter le bilan et d’envisager la prise en charge dans des conditions optimales. En cas de cœlioscopie réalisée dans le cadre de l’urgence (suspicion de salpingite, de torsion d’annexe, ou de complication de kyste), la chirurgie d’exérèse des lésions d’endométriose de découverte peropératoire n’est pas recommandée.

-L’hystérographie n’a plus d’indication pour le diagnostic mais si elle est réalisée dans le cadre d’une infertilité elle peut montrer de signes d’adénomyose ou d’endométriose tubaire: diverticules rectilignes, courts, terminés en massue, ectasie d’une corne, ectasie généralisée, bord rigide en ligne brisée, Partie initiale des trompes verticale (en lampe d’Aladin; tuba erecta), images d’addition tubaires en boules de gui.
Enfin, depuis 2022, la start-up lyonnaise Ziwig a développé un tel salivaire simple à réalise, permettant un séquençage à haut débit des petits ARN pour identifier les microARN particulièrement exprimés chez les femmes présentant un diagnostic d’endométriose. De ces données ont été extraites les valeurs d’expression des 109 microARN précédemment identifiés. Ce test a une forte sensibilité (96 %) et une forte spécificité (95 %). Il n’est pas remboursé par la SS.
Endométriose et infertilité
On pense qu’il existe par ailleurs des différences biologiques et physiologiques entre les femmes atteintes d’endométriose et les autres, qui seraient à l’origine de la baisse de fertilité souvent associée à cette maladie. Trois gènes sur les quatre codant pour les récepteurs aux prostaglandines, des médiateurs chimiques de l’inflammation, sont 10 à 20 fois plus exprimés dans l’endomètre utérin de patientes atteintes d’endométriose que dans celui de femmes qui ne présentent pas la maladie. Ce taux est même multiplié par quarante dans les tissus endométriaux extraits de lésions. En parallèle, l’expression d’une enzyme clef de la synthèse des prostaglandines, la PTGS2, est augmentée près de 10 fois dans l’endomètre des patientes endométriosiques. D’autres pistes biologiques paraissent pertinentes à explorer pour comprendre l’infertilité de ces patientes, comme celle de la fonction et de la réserve ovarienne des femmes atteintes d’endométriose.
Plusieurs études pointent en outre du doigt l’existence de facteurs de risque environnementaux. Les chercheurs s’interrogent par exemple sur le rôle éventuel des perturbateurs endocriniens ou celui de l’influence des acides gras polyinsaturés et d’autres composants alimentaires pouvant entrainer des anomalies épigénétiques.
Classification
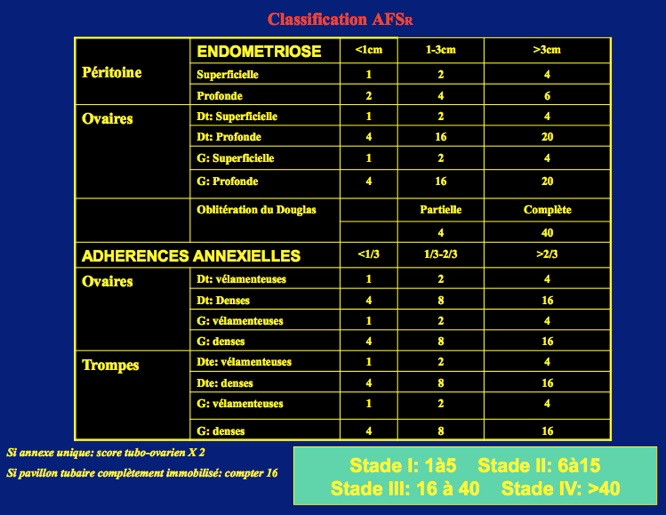
Traitements de l’endométriose
(inspiré des recommandations du CNGOF(Collège National des Gynécologues et Obstétriciens Français)
Voir également: https://www.aphp.fr/patient-public/endometriose/recommandations-endometriose/prise-en-charge-medicamenteuse-de
Une endométriose asymptomatique, non douloureuse et qui ne pose pas de problèmes de fertilité n’est en général pas détectée et donc pas traitée. Le traitement peut selon les cas faire appel à des médicaments favorisant une atrophie des lésions d’endométriose mais des traitements chirurgicaux par cœlioscopie sont aussi pratiqués. Cependant, malgré les divers traitements , l’endométriose reste une maladie capricieuse, difficile à guérir et parfois fortement évolutive malgré tous les traitements possibles. Une seule chose est garantie : elle guérit définitivement à la ménopause.
Le choix du traitement dépend du désir de grossesse, de l’âge et de la gravité et de l’étendue des lésions.
A-Prise en charge d’une endométriose douloureuse
Les lésions d’endométriose retrouvées ne sont pas toujours la seule étiologie des douleurs dont souffrent les patientes. Des facteurs psychologiques peuvent influencer l’importance de la douleur chez les femmes porteuses d’endométriose. La douleur de l’endométriose peut entraîner des altérations de la personnalité. La prise en charge psychologique des patientes souffrant de douleurs pelviennes chroniques améliore les résultats du traitemen. L’approche multidisciplinaire est recommandée dans la prise en charge des douleurs associées à l’endométriose.
Un traitement hormonal ou chirurgical doit être proposé en cas d’endométriose douloureuse. Le traitement médical a un effet suspensif sur les douleurs et sur la maladie mais certaines lésions peuvent échapper ou ne pas répondre au traitement médical. Il n’a pas d’effet «curatif» mais seulement un effet suspensif pendant la durée du traitement. Chez les patientes présentant des douleurs d’endométriose, un traitement médical hormonal visant à l’obtention d’une aménorrhée (contraceptifs œstroprogestatifs monophasiques en continu, progestatifs, danazol ou analogues de la Gn-RH) est utile dans le but de traiter les symptômes douloureux de l’endométriose. La prescription des analogues de la Gn-RH ne devrait pas être prolongée au-delà de 1 an.
De nouveaux outils de diagnostic de l’endométriose moins invasifs, basés sur des questionnaires ou sur des outils de biologie moléculaire couplés à l’intelligence artificielle, sont en cours de validation. Les progestatifs macrodosés, largement utilisés jusque-là pour traiter l’endométriose, sont remis en cause du fait d’un sur-risque de méningiome. Le diénogest est un progestatif efficace dans le traitement de la douleur liée à l’endométriose, la diminution des lésions ovariennes et la prévention des récidives postopératoires. Il n’a pas été mis en évidence de risque de méningiome sous diénogest dans la pharmacovigilance allemande.De nouveaux antagonistes oraux de la GnRH, associés ou non une add-back therapy, sont en cours de développement pour le traitement de l’endométriose.
Le traitement chirurgical de l’endométriose est en principe efficace sur les symptômes douloureux. Il est efficace s’il est complet, c’est-à-dire s’il retire la totalité des lésions. Sa réalisation est recommandée en cas d’endométriose douloureuse, sous réserve d’un rapport bénéfice risque individuel favorable. Le traitement chirurgical a donc une valeur curative surtout pour les femmes présentant des formes localisées, profondes, avec des lésions peu nombreuses mais bien définies, et dont la relation avec les symptômes douloureux est certaine, et dont l’exérèse complète apporte un bénéfice indiscutable. Bien que le risque de récidives postopératoires soit réel, pour ces femmes la résection complète des lésions permet une amélioration significative des douleurs et de la qualité de vie, au moins à court et moyen terme. En revanche, dans les formes étendue de la maladie, comportant des dizaines ou des centaines d’implants millimétriques dispersés sur tout le péritoine de la cavité abdomino-pelvienne et jusqu’aux coupoles diaphragmatique, la réalisation d’une chirurgie complète et curative reste simplement un vœux pieux. Pour ces dernières patientes, qui sont parfois classées dans les stades 1 et 2 AFSr, la chirurgie n’apporte qu’un bénéfice mineur et de courte durée, car plus de 50% de femmes seront de nouveau douloureuses au cours des mois ou des années suivantes.
Un traitement qui se veux complet expose toutefois à des complications chirurgicales et devrait être réalisé dans un centre «expert » .
Lors de la découverte d’un endométriome chez une patiente présentant des douleurs d’endométriose, il est recommandé de rechercher et traiter en même temps les autres localisations de l’endométriose.
Il n’existe pas de données permettant de comparer les résultats, sur le moyen et long terme, du traitement médical exclusif prolongé et du traitement chirurgical (avec ou sans traitement médical adjuvant).
En cas de récidive postopératoire des douleurs, un traitement médical peut être instauré (accord professionnel). L’hystérectomie totale avec annexectomie bilatérale et exérèse des implants est une option efficace sur les récidives des douleur.
B-Le cas des endométriomes
L’indication chirurgicale est difficile à poser car :
-Le traitement médical est très peu efficace sur les douleurs liées à l’endométriome, et plutôt inefficace quant à l’amélioration de la fertilité.
-une abstention thérapeutique, peut favoriser une destruction du parenchyme ovarien (baisse de la réserve ovarienne) et laisser persister la symptomatologie fonctionnelle (douleurs pelviennes, dysménorrhée)
-Une prise en charge chirurgicale, même unilatérale, peut aussi altérer la fonction ovarienne du fait des difficultés de dissection de ces kystes (résection excessive de parenchyme sain, inflammation postopératoire, destruction thermique par coagulation du hile, séquelles adhérentielles) avec abaissement post opératoire des taux d’AMH (réserve ovarienne).
Si le traitement chirurgical est choisi, le geste de première intention est la kystectomie coelioscopique. Compte tenu des difficultés de dissection de ces kystes, on observe toujours un effet délétère sur la réserve ovarienne.
En cas de chirurgie particulièrement difficile, gros kyste de plus de 8 à 10cm, fortes adhérence, dissection hémorragique, plutôt qu’une laparoconversion, il est préférable, après aspiration du kyste et lavage soigneux, de re-intervenir après 3 mois de traitement et avant le retour des règles, par analogues du GnRH.
Dans le cadre de la PMA, si la kystectomie cœlioscopique est le traitement chirurgical de première intention de l’endométriome, le bénéfice d’une telle chirurgie avant AMP reste controversé. En effet, les résultats des tentatives de FIV ne semblent pas altérés par la présence d’une endométriose ovarienne et les complications potentielles ( infection des endométriomes lors des ponctions (justifiant une mise en route systématique d’une antibioprophylaxie), contamination des ovocytes par le liquide de l’endométriome, difficulté d’accès aux ovocytes) sont très rares et n’impactent pratiquement pas ou peu les résultats. Le traitement médical peut limiter le dévelo pement du kyste ou même diminuer sa taille, mais cet effet ne contribue pas à la réduction du tissu endométriosique. Il en résulte que le traitement médical ne peut être préconisé pour la prise en charge des endométriomes en cas d’infertilité.
Bien que les chances de grossesse spontanée chez les patientes candidates à l’AMP puissent augmenter avec la chirurgie de l’endométriome, il faut souligner que le bénéfice de cette chirurgie reste limité dans ce contexte.
Les arguments en faveur de la chirurgie peuvent être:
-Risque de carcinome ovarien ou de tumeur borderline méconnue.
-Développement d’abcès pelvien après ponctions ovocytaires.
-Risque de rupture du kyste endométriosique, de contamination du liquide folliculaire, de difficultés lors de la ponction ovocytaire.
-La crainte de complications obstétricales : accouchement prématuré et retard de croissance intra-utérin dans certains cas particuliers.
Chez les patientes infertiles et asymptomatiques, et notamment parmi elles les plus âgées, celles dont la fonction ovarienne semble déjà entamée (avec abaissement de la réserve ovarienne), qui ont déjà des antécédents de chirurgie pelvienne ou une atteinte ovarienne bilatérale, il semble préférable d’envisager d’emblée une prise en charge par FIV.
En revanche pour les patientes les plus jeunes, présentant des douleurs pelviennes, une lésion unilatérale de plus de 6cm et une bonne réserve ovarienne ou une suspicion de lésion atypique (ou qui ne désirent plus ou pas d’AMP) une exploration et une prise en charge chirurgicale peut être utile. Par la suite, dans l’hypothèse d’une récidive de l’endométriome malgré une exérèse bien conduite, la bonne attitude consiste à s’abstenir de toute nouvelle intervention.
C-Prise en charge de l’infertilité associée à l’endométriose
1-En première intention
L’endométriose minime ou légère est parfois responsable d’hypofertilité. Cette relation semble plus nette dans les stades 3 et 4. Aussi, dans le cadre d’un bilan d’infertilité, il est recommandé de recourir à la cœlioscopie en cas de suspicion clinique ou échographique d’endométriose, cela après un bilan échographique complet et de qualité.
En l’absence de signes évocateurs d’endométriose, le recours à des inséminations intra-utérines (IIU) est recommandé avant de proposer une cœlioscopie.
Lorsqu’une cœlioscopie est réalisée, le traitement chirurgical des lésions, s’il est possible, est recommandé pour améliorer la fertilité. Le bénéfice du traitement chirurgical est insuffisant dans les formes minimes et légères. Les avis sont partagés pour les formes modérées et sévères et pour l’endométriose sous-péritonéale profonde, les données sont insuffisantes pour conclure.
Après la chirurgie, les traitements médicaux postopératoires ne sont pas recommandés, en dehors du cas particulier d’orientation directe vers la fécondation in vitro. Le recours direct à la fécondation in vitro avant cœlioscopie, alors qu’il existe des arguments en faveur d’une endométriose, ne se justifie que dans de rares cas où la FIV aurait été indiquée de toute façon (antécédents de salpingectomie, stérilité masculine).
Si la cœlioscopie découvre des lésions extensives pour lesquelles la chirurgie expose à un risque élevé de complications, le recours direct à la FIV sans geste chirurgical est alors préférable. En l’absence de grossesse après chirurgie, la FIV permet d’obtenir une grossesse chez 50% des patientes.
Chez des patientes en dessous de 35 ans, et présentant des lésions minimes d’endométriose, la correction des facteurs d’infertilité (induction d’ovulation…) ou masculins modérés (insémination intra-utérine avec sperme du conjoint) est la première action thérapeutique à envisager. Chez des patientes de plus de 35 ans,on aura recours à l’insémination avec sperme du conjoint et très vite, en cas d’échec, à la fécondation in vitro (FIV). Enfin chez les patientes présentant une endométriose de stade III ou IV, avec endométriome ovarien, il n’est pas prouvé que la chirurgie par kystectomie ovarienne augmente les résultats de la FIV et les taux de grossesse.
2-En deuxième intention
Après une chirurgie satisfaisante chez une patiente ne présentant pas d’autres facteurs négatifs, il est recommandé de respecter un délai d’attente de 6 à 12 mois avant de proposer une nouvelle thérapeutique . Ce délai est à moduler en fonction de l’âge de la patiente et des autres facteurs d’hypofertilité.
La chirurgie itérative n’est pas recommandée pour la seule raison d’une infertilité persistante après la chirurgie.
La stratégie du traitement de seconde ligne dépend du stade de l’endométriose et des facteurs associés. En présence d’un facteur mécanique évident (stade III-IV ou atteinte tubaire), la FIV est recommandée. Dans les autres cas, plusieurs options sont possibles : stimulation de l’ovulation, insémination intra-utérine . En cas d’échec de ces traitements, le recours à la FIV est recommandé. Il est recommandé de retraiter l’endométriose médicalement par les analogues de la Gn-RH avant d’entreprendre une FIV.
3-Endométriomes et FIV
Les endométriomes n’ont pas d’impact sur le résultat final d’une FIV. La découverte d’un endométriome lors d’une stimulation de FIV ne doit pas conduire à l’interruption de la tentative. Pour les endométriomes de moins de 6 cm, ni le traitement chirurgical itératif ni la ponction des endométriomes ne sont recommandés avant la FIV .
4-Douleur et infertilité
En cas d’association d’une infertilité et de douleurs persistantes (ou récidivantes) après traitement chirurgical initial, il est recommandé d’éviter autant que possible une nouvelle chirurgie. La mise sous traitement hormonal (œstroprogestatifs en continu, progestatifs ou analogues de la Gn-RH) entre les tentatives d’AMP doit être préférée.
C-Méthodologie de la prise en charge chirurgicale
1-Choix de la voie d’abord
La cœlioscopie est la voie d’abord de choix pour le traitement des endométriomes ovariens et de l’endométriose péritonéale superficielle.
La faisabilité de la cœlioscopie ou de la voie vaginale cœlio-assistée a été démontrée, entre des mains expertes, pour toutes les formes d’endométriose sous-péritonéale profonde. La voie vaginale exclusive n’est pas recommandée dans le traitement de l’endométriose sous-péritonéale profonde. Toutefois, si l’exérèse complète des lésions est l’objectif, une chirurgie complète par laparotomie est toujours préférable à une chirurgie incomplète par cœlioscopie.
2-Chirurgie de l’endométriose péritonéale superficielle
Les deux techniques cœlioscopiques : destruction (coagulation, vaporisation laser), ou exérèse des lésions sont efficaces dans le traitement de l’endométriose superficielle.
3-Chirurgie des kystes endométriosiques de l’ovaire
La ponction échoguidée n’est pas le traitement de première intention. Le drainage percœlioscopique simple n’est pas recommandé car il conduit à une récidive immédiate.
La kystectomie intrapéritonéale est supérieure au drainage suivi de la destruction de la paroi du kyste par coagulation bipolaire, pour les endométriomes d’au moins 3 cm de diamètre, quel que soit le but du traitement du kyste (infertilité, douleur ou masse annexielle). La kystectomie doit être réalisée à chaque fois qu’elle est techniquement possible.
La stratégie en trois temps : cœlioscopie diagnostique et drainage, puis traitement médical par les analogues, puis deuxième cœlioscopie d’exérèse semble comparable au traitement en un seul temps en termes de récidives, de grossesses, de limitation des adhérences. Cette approche constitue une alternative lorsque la chirurgie en un temps est trop difficile.
L’annexectomie ou l’ovariectomie n’est une alternative à la Kystectomie que chez la femme qui ne souhaite plus d’enfant ou qui a récidivé.
La prescription d’un traitement médical par les analogues de la Gn-RH n’est pas recommandée en préopératoire dans le but de faciliter la chirurgie des endométriomes.
4-Chirurgie des lésions d’endométriose sous-péritonéale profonde
Il est recommandé que les lésions les plus sévères soient traitées par des équipes expérimentées dans la prise en charge de l’endométriose. La chirurgie d’exérèse des lésions d’endométriose sous-péritonéale profonde de la cloison recto-vaginale (y compris vagin ou utéro-sacrés) sans atteinte rectale permet une amélioration des douleurs d’endométriose chez 60 à 100 % des patientes. La chirurgie d’exérèse est recommandée en raison de son efficacité à moyen terme sur les symptômes douloureux . Les résultats à long terme ne sont pas évalués.
La chirurgie d’exérèse des lésions d’endométriose sous-péritonéale profonde postérieure avec atteinte digestive permet une amélioration significative des douleurs d’endométriose. Il n’y a de consensus ni sur la technique ni sur la radicalité d’exérèse qu’il faut utiliser dans le traitement des lésions d’endométriose sous-péritonéale profonde avec atteinte digestive.
La cystectomie partielle est recommandée pour le traitement des lésions d’endométriose sous-péritonéale profonde infiltrant la paroi vésical. La résection transurétrale n’a pas de place dans le traitement chirurgical de l’endométriose vésicale.
5-Chirurgie adjuvante de la douleur
L’hystérectomie simple (avec la conservation des ovaires et sans l’exérèse des implants) n’est pas recommandée en raison du risque élevé d’échec sur la douleur. La conservation ovarienne est associée à un risque majoré de récidive. Mais la place de la castration chirurgicale ne peut être précisée en l’absence de données.
La section isolée de l’origine des ligaments utéro-sacrésn’est pas recommandée dans la prise en charge de l’endométriose douloureuse. Les données actuelles sont insuffisantes pour recommander la neurectomie présacrée dans le traitement de l’endométriose douloureuse.
Les données disponibles ne permettent pas de recommander la réalisation isolée d’une adhésiolyse dans le traitement des douleurs d’endométriose.
L’utilisation de certains produits barrières anti-adhérences dans la chirurgie de l’endométriose est efficace dans la prévention de la reformation des adhérences pelviennes .
6-Les complications de la chirurgie de l’endométriose
L’incidence des complications majeures de la chirurgie pour endométriose est de l’ordre de 0,1 à 15 % en fonction de l’importance des lésions. Les taux les plus élevés sont observés dans la prise en charge de l’endométriose sous-péritonéale profonde. Ces complications peuvent notamment compromettre la fertilité spontanée. La patiente doit être informée du risque de ces complications spécifiques graves et de leurs implications possibles sur la fertilité. Il est souhaitable d’expliquer que l’amélioration des douleurs n’est pas constante après la chirurgie.
D-Formes particulières d’endométriose et cas particuliers de la prise en charge
1-Endométriose pariétale
Le diagnostic préopératoire repose sur l’IRM. Le traitement chirurgical est recommandé et consiste en une résection large de la masse. Il n’est pas recommandé de réaliser une cœlioscopie à la recherche de lésions pelviennes.
2-Endométriose appendiculaire
L’endométriose appendiculaire est une localisation fréquente de l’endométriose digestive. Lorsqu’une cœlioscopie est réalisée dans le cadre d’un bilan d’endométriose, il n’y a pas de données permettant de recommander l’exérèse de l’appendice dans le même temps opératoire. Dans le cas particulier d’une cœlioscopie pour douleur, la présence de lésions profondes, responsables d’une induration ou d’une rigidité de l’appendice, justifie l’appendicectomie.
3-Endométriose pleurale
La survenue d’un pneumothorax ou d’un hémothorax en période périmenstruelle doit faire évoquer le diagnostic d’endométriose pleurale.
Le diagnostic de certitude repose sur la thoracoscopie, mais cet examen ne permet pas de poser le diagnostic d’endométriose pleurale dans 100 % des cas . Cet examen n’est pas recommandé en première intention.
Le traitement de l’endométriose pleurale vise, dans un premier temps médical, à traiter le pneumothorax initial et à éviter les récidives ultérieures par l’obtention d’une aménorrhée thérapeutique de longue durée . En cas d’échec, le traitement est chirurgical et doit associer pleurodèse et traitement chirurgical des lésions .
4-Endométriose pulmonaire
L’endométriose pulmonaire est une localisation très rare, le diagnostic d’endométriose pulmonaire est évoqué par le caractère cataménial des symptômes . Les examens complémentaires à visée diagnostique (bronchoscopie, scanner, IRM) doivent être réalisés lors des menstruations, ce qui améliore la probabilité du diagnostic d’endométriose pulmonaire.
La place respective du traitement médical et du traitement chirurgical dans l’endométriose pulmonaire est difficile à préciser en l’absence de données comparatives.
5-L’endométriose diaphragmatique
La douleur cataméniale pulmonaire droite ou de l’épaule droite doit faire évoquer le diagnostic d’endométriose diaphragmatique. La cœlioscopie conventionnelle ne permet pas toujours de visualiser les lésions qui peuvent être situées au niveau de la partie postérieure du diaphragme. Les traitements médicaux et chirurgicaux semblent efficaces, mais les données sont insuffisantes pour proposer une stratégie de prise en charge.