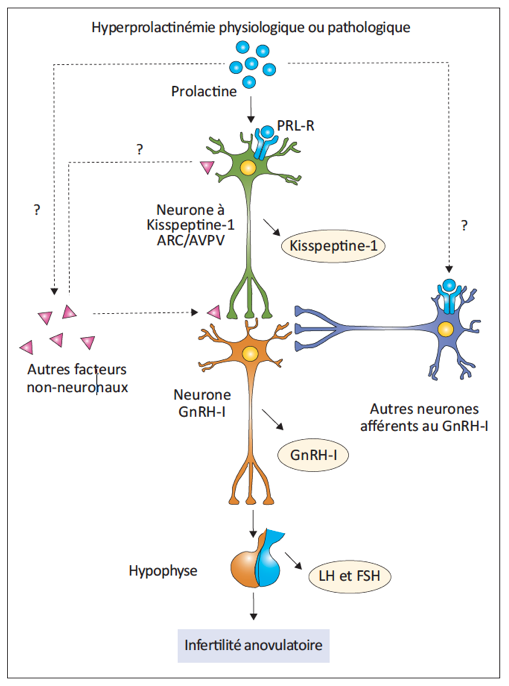
Le rôle principal de la prolactine est d’assurer la lactation chez la femme. La sécrétion de prolactine est sous le contrôle principal du tonus inhibiteur de la dopamine d’origine hypothalamique. Toute interruption de ce tonus inhibiteur, qu’elle soit fonctionnelle (médicaments) ou organique (lésion de la région hypothalamo-hypophysaire) peut provoquer une hyperprolactinémie. L’hyperprolatcinémie entraîne une diminution de la kisspepine-1 et de ce fait, une diminution de la sécrétion de GnRH, responsable d’une insuffisance gonadotrope ayant pour conséquences une hypoestrogénie chronique et une infertilité.
Le dosage de la prolactine
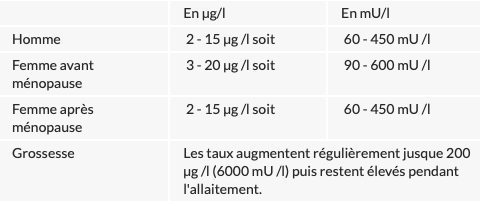
Après avoir été un temps discuté, il est maintenant admis que le dosage ne nécessite qu’une seule prise, pas forcément à jeun en évitant simplement les traumatismes veineux. On ne fait plus de tests dynamiques. Cela même si l’on sait que le taux de prolactine varie au cours de la journée. Le pic a lieu au cours du sommeil (0 à 7 heures). On constate également un pic post-prandial (après le repas). La sécrétion est pulsatile toutes les 20 minutes. Le stress, l’exercice physique, l’hypoglycémie ou même la crainte de la prise de sang peuvent provoquer des augmentations de la prolactine.
L’hyperprolactinémie est définie par un taux de prolactine supérieur à la limite supérieure de la norme du laboratoire, en général entre 20 et 25 ng/ml chez la femme.
Rôle de la prolactine
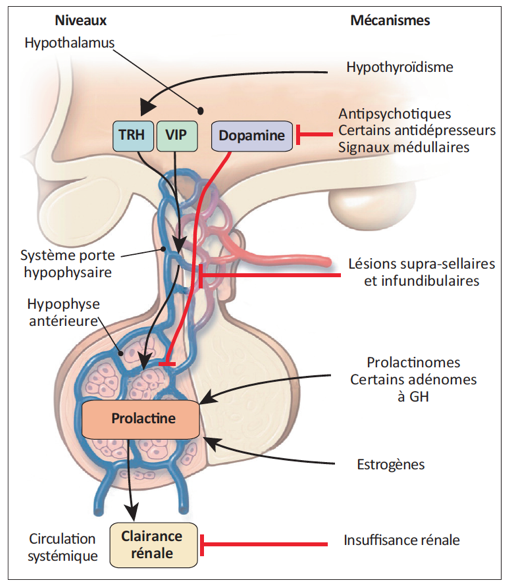
La prolactine est synthétisée et sécrétée par les cellules hypophysaires lactotropes. Cette synthèse et cette sécrétion sont sous le contrôle du tonus inhibiteur de la dopamine d’origine hypothalamique, qui traverse le système veineux portal pour agir sur les récepteurs D2 des cellules lactotropes. La synthèse et la sécrétion de prolactine sont simulées par les estrogènes, la TRH (thyrotropin releasing hormone), l’EGF (epidermal growth factor), les antagonistes du récepteur à la dopamine et plus largement par tout ce qui interfère avec le tonus inhibiteur dopaminergique. Le rôle principal de la prolactine est d’induire et de maintenir la lactation en simulant la prolifération et la différenciation des cellules mammaires. La PRL joue également un rôle dans le développement de la glande mammaire à la puberté, mais aussi dans la reproduction (rôle sur l’ovaire, l’utérus). Son implication est aussi démontrée chez l’animal, dans la croissance, le développement, le comportement, l’osmorégulation et l’immunomodulation.
Les causes de l’hyperprolactinémie
Outre les causes physiologiques comme la grossesse ou l’allaitement, de nombreuses substances pharmacologiques peuvent être responsables d’une hyperprolactinémie par le biais de divers mécanismes. Ainsi, un certain nombre de neuroleptiques bloquent les récepteurs à la dopamine. Certains antidépresseurs induisent une inhibition sérotoninergique des neurones à dopamine. Des médicaments gastro-intesinaux, comme la cimétidine ou le métoclopramide sont antidopaminergiques. Plusieurs molécules ani-hypertensives (la méthyldopa, la réserpine, le vérapamil) diminuent la synthèse de dopamine. Les opiacés sont également pourvoyeurs d’hyperprolactinémie. La liste n’est pas exhaustive, et on n’oubliera pas les estrogènes qui simulent directement la croissance des cellules lactotropes et la sécrétion de PRL. L’hypothyroïdie profonde, par le biais de l’augmentation de la TRH, augmente aussi la sécrétion de PRL. L’insuffisance rénale chronique, par le biais notamment de la diminution de sa clairance rénale, augmente les taux circulants de prolactine.
Toutes les pathologies entraînant des lésions suprasellaires et infundibulaires, interférant avec le transport de la dopamine hypothalamique, via le système porte, vers l’hypophyse, sont responsables d’une hyperprolactinémie dite « de déconnexion ». Enfin, les prolactinomes, tumeurs impliquant les cellules lactotropes antéhypophysaires, sont une des principales étiologies d’hyperprolactinémie.
Conséquences de l’hyperprolactinémie
Les signes cliniques de l’hyperprolactinémie sont les troubles du cycle (spanioménorrhée, aménorrhée), la galactorrhée et l’infertilité. L’hyperprolactinémie est responsable d’un hypogonadisme hypogonadotrope fonctionnel, ayant comme conséquences une infertilité anovulatoire et une hypoestrogénie chronique. Dans les causes hypophysaires, surtout en cas de macro-adénome, on retrouve classiquement des céphalées et parfois des troubles visuels en cas de tumeur comprimant les voies optiques.
Conduite à tenir devant une hyperprolactinémie
Devant un dosage de prolactine élevé, notamment en l’absence de troubles du cycle, il faut d’abord éliminer une macroprolactinémie. En effet le dosage de la prolactine peut être faussé par la présence de ces macromolécules de prolactine. On utilise alors une technique de précipitation au polyéthylène-glycol (PEG) qui permet de ne doser que la forme active de la prolactine.
Ensuite, il faut par un interrogatoire minutieux, rechercher la prise de médicaments hyperprolactinémiants. Si tel est le cas, il faudra discuter la possibilité d’arrêter ce traitement de façon à pouvoir contrôler la prolactine à distance. Si un tel arrêt n’est pas envisageable, il faudra alors réaliser une IRM hypophysaire afin d’éliminer une lésion de la région hypothalamo-hypophysaire.
Il faut toujours penser à rechercher une situation d’hyperestrogénie, qui pourrait expliquer l’hyperprolactinémie modérée. On vérifiera donc l’absence de grossesse, d’allaitement, de prise de pilule estroprogestative ou de traitement hormonal substitutif contenant des estrogènes.
Il conviendra d’éliminer une insuffisance rénale chronique ainsi qu’une hypothyroïdie périphérique profonde.
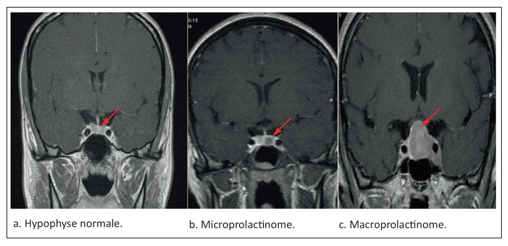
Enfin, on réalisera une IRM hypophysaire à la recherche d’un microprolactinome, d’un macroprolactinome, d’une section de tige, d’un kyste de la poche de Rathke ou de toute autre lésion hypothalamo-hypophysaire pouvant être responsable d’une hyperprolactinémie de déconnexion.
En cas d’hyperprolactinémie médicamenteuse, on envisagera d’abord l’arrêt du traitement avec éventuellement un changement de molécule pour un traitement non hyperprolactinémiant. Si l’arrêt du médicament hyperprolacinémiant n’est pas envisageable, deux cas de figure :
– soit il est possible d’adjoindre un traitement par agoniste dopaminergique,
– soit ce n’est pas possible et, dans ce cas, il faudra envisager un traitement estrogénique substitutif pour pallier les conséquences de l’hypoestrogénie chronique. En effet, dans le cas des traitements psychiatriques hyperprolactinémiants, comme les neuroleptiques, l’agoniste dopaminergique risque d’aggraver le tableau psychiatrique ; il conviendra donc de bien peser la balance bénéfices-risques d’un traitement par agoniste dopaminergique avec le psychiatre.
Dans le cas d’un adénome à prolactine, la prise en charge dépend de la taille de l’adénome et du statut ménopausique ou non de la femme.
– S’il s’agit d’un macroprolactinome, que la femme soit ménopausée ou non, le traitement de première intention sera toujours la mise en route d’un traitement agoniste dopaminergique.
– S’il s’agit d’un microprolactinome, 3 situations :
• la femme est non ménopausée et souhaite une grossesse : on proposera en première intention un traitement par agoniste dopaminergique ;
• la femme est non ménopausée et ne souhaite pas de grossesse : on proposera une contraception estroprogestative (qui permettra de corriger la carence estrogénique) ;
• la femme est ménopausée : il n’y a pas d’indication à traiter puisque le volume de l’adénome n’est pas menaçant et que les conséquences de l’hyperprolactinémie sur l’axe gonadotrope ne sont plus une préoccupation. Il n’y a bien sûr pas de contre-indication à un traitement hormonal substitutif de la ménopause.

Les agonistes dopaminergiques ont deux foncions : la diminution de la sécrétion de prolactine et la diminution du volume tumoral. L’objectif est la restauration de la fonction gonadotrope chez la femme non ménopausée ; si ce n’est pas le cas, il faudra discuter la mise en place d’un traitement substitutif estroprogestaif.
Parmi les agonistes dopaminergiques disponibles, celui à utiliser en première intention est la cabergoline (Dostinex®) car il est le plus efficace, le mieux toléré et présente une longue durée d’action autorisant des prises hebdomadaires. Il présente donc l’avantage d’une meilleure observance. De plus, il a maintenant bien été démontré qu’aux doses utilisées en endocrinologie, il n’y a pas de risque de valvulopathie. Il n’est donc pas nécessaire de surveiller l’échographie cardiaque. Enfin, la littérature est très rassurante quant à son utilisation pendant la grossesse. Il est recommandé d’arrêter la cabergoline dès le diagnostic de grossesse, sauf en cas de macroprolactinome menaçant les voies visuelles, auquel cas le traitement sera poursuivi. La prise de cabergoline empêche évidemment l’allaitement, mais si ce traitement n’est pas nécessaire pendant la grossesse, il n’y a pas de contre-indication à l’allaitement et le traitement pourra être repris après le sevrage.
Si la cabergoline est mal tolérée ou inefficace malgré une augmentation des doses, on pourra la remplacer par le quinagolide (Norprolac®), voire par la bromocripine (Parlodel®), mais ce dernier est souvent mal toléré.
La chirurgie d’un prolactinome peut se discuter en cas d’intolérance ou d’inefficacité réelle des agonistes dopaminergiques.